网站首页健康养生 >正文
胰腺导管腺癌(PDAC)是最常见的胰腺癌形式。超过90%的PDAC患者在诊断后五年内死亡。通常,当癌症被发现时,它已经扩散了。冷泉港实验室(CSHL)的研究人员试图了解PDAC的潜在遗传机制。他们探索了RNA剪接在胰腺癌中的作用,发现高水平的剪接调节蛋白SRSF1会导致胰腺炎并促进PDAC肿瘤的发展。
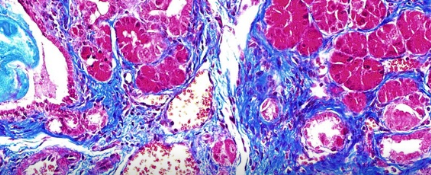
他们的研究结果发表在《CancerDiscovery》杂志上一篇题为“剪接因子SRSF1促进胰腺炎和KRASG12D介导的胰腺癌”的文章中。
研究人员写道:“炎症与PDAC这种高度致命的恶性肿瘤密切相关。”“RNA剪接因子失调在肿瘤发生中已被广泛报道,但它们在胰腺炎和PDAC中的作用尚不清楚。在这里,我们报道剪接因子SRSF1在胰腺炎、PDAC前体病变和肿瘤中高表达。SRSF1的增加足以诱发胰腺炎并加速KRASG12D介导的PDAC。”
CSHL教授AdrianKrainer博士解释说:“PDAC通常发现得太晚,化疗和手术等治疗效果不佳。”
Krainer和CSHL博士后LedongWan博士与CSHL教授DavidTuveson博士合作,探索胰腺癌中的RNA剪接。
“细胞有几个过程来保持SRSF1水平恒定,”Krainer说。“但癌症往往会找到一种方法来克服这些制衡。”
多种基因、RNA和蛋白质在细胞中共同作用,以保持SRSF1水平稳定。然而,当胰腺中的这一过程受到干扰时,就会引发胰腺炎并加速PDAC。
“这是一个非常明显的效果,”克莱纳解释道。“我们可以看到,肿瘤中SRSF1表达水平较高的患者预后较差。因此,我们开始探索SRSF1对PDAC的贡献有多大。”
研究小组发现,较高水平的SRSF1对于小鼠和类器官(小型肿瘤)的PDAC生长至关重要。当SRSF1恢复到正常水平时,类器官停止生长。SRSF1在健康组织中很重要,因此它本身可能不是理想的治疗靶点。然而,它所促进的一些剪接变化可能是有针对性的。
“我们对这些进展感到兴奋,”他说。“但PDAC是一种困难且复杂的恶性肿瘤。我们希望为未来的治疗提供可操作的信息。乐东牵头的这项工作只是冰山一角。”
版权说明:本站所有作品图文均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系我们
相关文章:
- 2023-11-26贻贝组织和足丝之间的动态生物界面在快速释放中发挥重要作用
- 2023-11-24研究人员采用新的人工智能方法来分析肿瘤
- 2023-11-24干细胞研究为骨骼肌再生铺平道路
- 2023-11-24使用人工智能了解健康的老年人如何在家中度过老年
- 2023-11-24研究表明植物利用空气通道产生定向光信号并调节向光性
- 2023-11-24科学家们最终通过溶解生长过程中的结构缺陷成功在实验室中生长白云石
- 2023-11-24荷兰退休人员帮助解开蝙蝠阴茎异常大之谜
- 2023-11-23这条海虫的后部游走了现在科学家知道了它是如何做到的
- 2023-11-23以人工智能为指导更好地制造钙钛矿太阳能电池
- 2023-11-23从废煤中提取碳纤维
- 站长推荐
- 栏目推荐
- 阅读排行
- 健康和教育密切相关新西兰需要将其更多地融入小学
- Steam现已全面支持DualShock和DualSense控制器无需购买新的Xbox控制器
- DistrictTaco希望扩大其在罗利地区的业务
- Humane的AiPin–您的新型可穿戴人工智能助手
- Microsoft365CopilotAI如何提高您的工作效率
- MicrosoftRadius云开源应用程序平台
- 生产目的FiskerPear具有透明A柱因为移动头部太困难
- 索尼Xperia5V马来西亚发布Snapdragon8Gen2SoC 8GBRAM 256GB储存空间起价RM4999
- Nissan的模块化PulsarSportbak集轿跑车 旅行车和皮卡于一体
- 新奥尔良烤肉店将在中央市场推出
