网站首页健康养生 >正文
在蛋白质合成或翻译过程中,转录在细胞 mRNA 中的遗传信息会指导氨基酸(蛋白质的组成部分)的串联。当翻译机制沿着组成 mRNA 的核苷酸链移动时,它会以三组密码子为一组来识别它们。每个密码子对应一种特定的氨基酸。
某些密码子会告诉翻译机制从哪里开始和结束。但有时,就像闯红灯的违规司机一样,翻译机制会跳过终止密码子,最终生成比计划更长的蛋白质。这称为终止密码子通读。
印度科学研究所(IISc)生物化学系(BC)副教授桑迪普·埃斯瓦拉帕 (Sandeep Eswarappa) 解释道:“由于有了这个额外的附加物,蛋白质可以有不同的定位、不同的稳定性,甚至可以有不同的功能。”
在《细胞科学杂志》上发表的一项研究中,埃斯瓦拉帕的团队将注意力集中在一种名为 FEM1B 的蛋白质的编码基因上。他们展示了 FEM1B mRNA 读取如何在细胞周期中发挥关键作用,对癌细胞增殖和肿瘤生长有影响。
FEM1B 蛋白是标记其他蛋白质降解的复合物的一部分。它的作用是确保标记正确的蛋白质。该复合物靶向参与许多细胞过程的关键蛋白质,其中之一就是细胞周期,以控制细胞增殖的程度。
在这项研究中,研究人员发现,终止密码子通读会导致翻译机制产生更长、更不稳定的 FEM1B 版本。具有讽刺意味的是,这标志着 FEM1B 本身的降解,导致蛋白质水平降低。研究小组发现,FEM1B 基因尾端的特定核苷酸序列指导了这种通读。
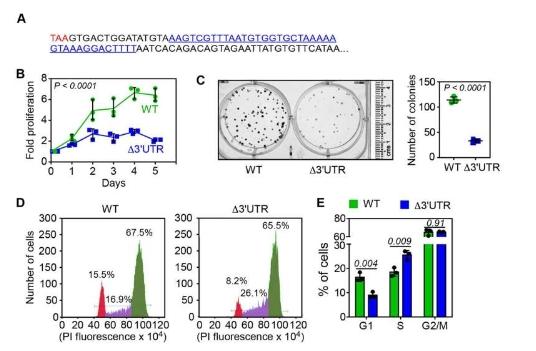
随后,研究小组开始好奇这会如何影响癌细胞的生长——这种致命疾病的一个特点是细胞不受控制地增殖。在实验室培养的癌细胞系中,他们部署了 CRISPR-Cas9 系统——常用的“分子剪刀”——从 FEM1B 基因中剪掉驱动读通的序列。
阻止通读会导致 FEM1B 蛋白水平升高,从而增加靶蛋白的降解,并延迟细胞周期。这导致癌细胞增殖减少。
“这很令人惊讶,因为它为这项研究带来了临床意义,”主要作者、Eswarappa 实验室综合博士生 Md Noor Akhtar 说道。该团队随后将有读通缺陷的癌细胞系注射到小鼠模型中,发现随之而来的肿瘤生长得更慢。
通过深入研究人类癌症患者的公开数据集,研究人员还发现,FEM1B 基因表达水平越高,生存概率就越高,这与他们的假设一致。
当他们研究 FEM1B 基因的进化时,他们意识到,通读过程似乎只存在于人类和黑猩猩身上。他们认为,这种故障可能是由于在第一个终止密码子下游插入了一个核苷酸而发生的——这是一个微小的变化,发生在大约 1000 万年前,当时人类和黑猩猩与其他灵长类动物分道扬镳。
作者推测,这可能是导致人类与其他灵长类动物相比更容易患癌症的因素之一。
Eswarappa 的团队仍然对终止密码子读通究竟是如何发生的感到困惑。他们热衷于确定所涉及的分子机制,这将有助于使任何治疗方法更加具体。他补充说:“如果我们知道这种机制,我们就可以针对和调节读通过程,这反过来可能有助于控制肿瘤进展。”
版权说明:本站所有作品图文均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系我们
相关文章:
- 2024-09-10研究发现随着海洋变暖鲨鱼正在抛弃承受压力的珊瑚礁
- 2024-09-10基因分析揭示出现一种新的巨型毒牙蛙与体型更大的蛙种几乎完全相同
- 2024-09-10借助人工智能极端微生物揭示了生命构造模块如何适应高压
- 2024-09-10暂停生物钟可以促进实验室生产的血液干细胞
- 2024-09-09并行计算模型中的改进算法比现有的静态并行APSP算法速度更快
- 2024-09-09能阅读盲文的感官笔可以提高视障人士的识字能力
- 2024-09-09三一学院科学家获欧洲研究经费资助研究脑修复
- 2024-09-09脑肿瘤的尖峰电信号揭示被忽视的神经元神经胶质细胞杂交
- 2024-09-09免疫疗法促进小鼠脊髓损伤恢复
- 站长推荐
- 栏目推荐
