网站首页生活常识 >正文
在《科学报告》上发表的一份新报告中,MichaelJ.Rupar和美国佛罗里达州HesperosInc.的研究团队开发了一种功能性、多器官、无血清系统来培养恶性疟原虫——一种主要导致恶性疟原虫的原生动物。严重和致命的疟疾,以建立创新平台来开发治疗药物。
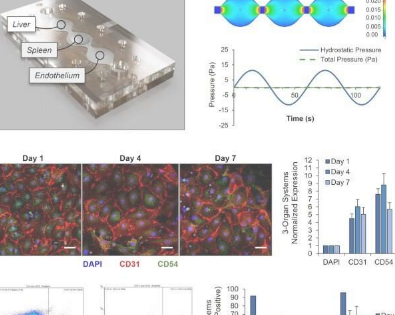
该平台包含四种人体器官构建体,包括肝细胞、脾细胞、内皮细胞和循环血细胞,用于与寄生生物体相互作用以模拟感染。研究小组使用了两种恶性疟原虫菌株:对氯喹敏感的3D7菌株;一种成熟的抗疟疾药物,以及W2菌株耐药的氯喹。他们在再循环微流体模型中将功能细胞维持在健康和患病条件下7天。
科学家们展示了一个有效的治疗开发平台,其中氯喹治疗可显着降低3D7菌株成分模型中的寄生虫血症。他们使用这种设置来确定治疗指数,以剂量依赖性方式评估抗疟疾治疗的脱靶毒性。结果可以建立一种新方法,在维持血液循环7天的真实人体模型中评估抗疟疾疗法。
恶性疟原虫的生命周期
寄生生命周期分为两个阶段:在吸血期间,子孢子从蚊子的唾液中释放出来,然后通过外周血液循环到达肝脏,在肝细胞内复制。这会在几天内产生大量的裂殖子,然后从破裂的肝细胞中释放出来,从肝脏进入血流。
裂殖子的生命周期是无性和红细胞的,寄生虫通过感染血细胞发育。由宿主血红蛋白推动的快速无性复制,导致裂殖子进入环状阶段,在48小时内成熟为滋养体和裂殖体,它们继续生长和复制直至破裂,释放更多的裂殖子以重复感染循环。
四器官疟疾芯片系统中恶性疟原虫的形态学进展。(a)添加3%原代人红细胞后的多器官外壳。(b)在系统组装当天,从连续培养物中提取受感染的红细胞,每个系统均以5-7%的寄生虫血症接种。根据薄血涂片和吉姆萨染色测定,恶性疟原虫的3D7和W2菌株在8天的时间内在系统中以2-6%的血细胞比容增殖。比例尺=5µm。(c)在多器官系统中培养四天后,观察到红细胞生命周期所有阶段的寄生虫,包括配子体形成第三阶段的寄生虫。(d)每12小时通过吉姆萨染色薄膜涂片测定寄生虫血症。当在4器官系统中共培养时,两种菌株的寄生虫血症在4-14%之间波动。数据点代表平均值±SEM。信用:科学报告,doi:10.1038/s41598-023-35694-4
抗疟疾战略的发展
疟疾是一种流行病,从2014年到2020年呈上升趋势,报告数量稳步增加,强调多年来耐药菌株的出现。因此,生物工程师和生命科学家热衷于开发抗疟疾的新方法,以对抗疾病的进展。
疟原虫寄生虫会引起疟疾,并由雌性按蚊传播。在这些变种中,恶性疟原虫是最致命的,是造成多种严重疟疾病例的主要原因。
世界卫生组织的目标是到2030年将全球疟疾病例发病率和死亡率降低90%。研究人员热衷于通过研究新平台来研究该疾病的治疗方法来实现这一目标。其中一项尝试是Rupar和同事开发了一种多器官、临床前抗疟疾药物发现平台,该平台可以建立并维持健康和疾病状况,作为动物模型的一种经济有效的方法。
实验设置
鲁帕尔等人。使用了两种恶性疟原虫菌株;一种对氯喹敏感且对氯喹耐药的菌株,在多器官模型中成功维持了8天。科学家们建立了这个仪器来评估人类疟疾治疗,检查该平台的效率和安全性,同时还探索治疗指数的安全性以进行进一步的研究。Rupar及其同事开发了一种包含三种成分的微流体装置,用于铺板肝脏、脾脏和内皮细胞。
无泵系统将重力驱动的流动引入具有正弦摇摆的多器官系统,并具有相关的生理参数。通过使用无泵的微流体设计疟疾芯片模型,他们确保了原代人类红细胞的再循环,以模拟恶性疟原虫全身感染的初级阶段。
(a)在4器官系统中与再循环的未感染或感染红细胞(RBC)共培养8天后,内皮、脾脏和肝脏器官构建体的形态。在所有条件下,寄生虫生长所需的红细胞浓度的存在使得这些器官模块的成像变得困难。然而,根据未感染(仅红细胞)和感染(3D7,W2)系统中器官之间明显的形态差异,培养物中恶性疟原虫的存在似乎会显着影响这些细胞的形态。(b–d)HUVEC、原代肝细胞和原代脾细胞的活力。没有观察到统计学上的显着差异;n=12。来源:科学报告,doi:10.1038/s41598-023-35694-4
疟疾芯片
科学家们通过在疟疾芯片平台上组装没有寄生虫的芯片上的细胞来表征多器官系统中的细胞。他们进行了为期7天的研究,以确定7天内健康微生理系统中的细胞活力、功能和外观。然后,该团队研究了仪器内寄生虫的生命周期,其中包括两种菌株:3D7菌株和W2菌株分别对氯喹敏感和氯喹耐药。
研究人员观察了8天的所有阶段,以确定每个系统中的寄生虫血症水平。
器官芯片仪器的实用性
研究小组接下来研究了器官芯片仪器中功能细胞的活力,其中含有被菌株或未感染血液感染的红细胞,培养了8天。他们利用相位成像在组装前和第8天分解后立即捕获了功能细胞。形态变化表明细胞活力在感染恶性疟原虫后受到破坏。
Rupar及其同事每12小时监测一次寄生虫血症,并注意到治疗组的寄生虫水平显着降低。尽管寄生虫水平的降低在药物敏感和耐药系统之间波动,但最终与耐药系统相比,氯喹敏感治疗组的水平明显较低。拆卸仪器后,他们继续研究组成细胞的活力。
外表
通过这种方式,MichaelJ.Rupar及其同事开发了代表恶性疟原虫感染的四器官疟疾疾病模型。利用该模型,研究小组确定了氯喹对器官结构功能或活力的任何脱靶影响,并确定了抗疟疗法的治疗指数。无血清多器官构建体包含肝脏、脾脏和内皮器官,为研究抗疟疗法提供了一种经济有效的方法。
这种结构使生物化学家和生物工程师能够在微生理器官芯片环境中实时研究寄生相互作用,并识别治疗化合物的可预见的脱靶效应。
版权说明:本站所有作品图文均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系我们
- 上一篇:羽毛球网高度标准尺寸,没有比这详细了!
- 下一篇:研究揭示植物再生的秘密
相关文章:
- 2023-11-26研究表明南极臭氧层空洞在仲春时更深
- 2023-11-24机器人假肢脚踝改善自然运动和稳定性
- 2023-11-24球形机器人来救援
- 2023-11-24解释人工智能的方法可能并不那么容易解释
- 2023-11-24描述开放系统中量子信息加扰的通用框架
- 2023-11-24研究为抗生素耐药性和健身景观提供了新的见解
- 2023-11-24物理学家发现量子材料中奇异电荷传输的证据
- 2023-11-23一种高效去除水产养殖废水中磷酸盐的方法
- 2023-11-23研究人员在防止钒电池容量损失方面获得了有希望的结果
- 2023-11-23了解化学处理沙土的强度发展机制
- 站长推荐
- 栏目推荐
- 阅读排行
- 健康和教育密切相关新西兰需要将其更多地融入小学
- Steam现已全面支持DualShock和DualSense控制器无需购买新的Xbox控制器
- DistrictTaco希望扩大其在罗利地区的业务
- Humane的AiPin–您的新型可穿戴人工智能助手
- Microsoft365CopilotAI如何提高您的工作效率
- MicrosoftRadius云开源应用程序平台
- 生产目的FiskerPear具有透明A柱因为移动头部太困难
- 索尼Xperia5V马来西亚发布Snapdragon8Gen2SoC 8GBRAM 256GB储存空间起价RM4999
- Nissan的模块化PulsarSportbak集轿跑车 旅行车和皮卡于一体
- 新奥尔良烤肉店将在中央市场推出
