网站首页生活常识 >正文
信使RNA(mRNA)疫苗正在彻底改变癌症治疗方法。它们可以在短时间内灵活开发,允许多种抗原的瞬时表达,从而实现安全高效的免疫。临床上正在探索多种mRNA疫苗,以使癌症患者受益。
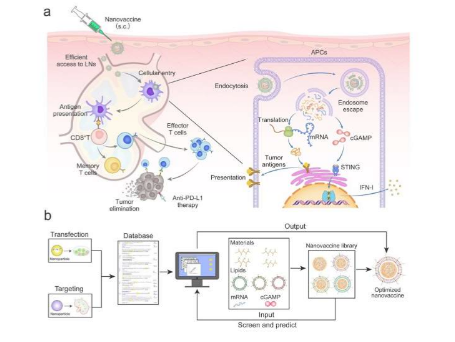
然而,mRNA疫苗的翻译在启动强免疫之前仍然受到多阶段传递障碍的阻碍,包括快速清除、对淋巴器官和树突状细胞的靶向性差的靶向性差、催化水解以及穿过磷脂双层的能力弱。此外,在没有佐剂的情况下,单独使用mRNA疫苗接种几乎不能诱导强烈的免疫反应。改善mRNA的胞质递送并与佐剂结合提高其体内疫苗接种功效仍然具有挑战性。
在过去的几十年里,大量的纳米载体被报道可以促进核酸药物的转染功效或将药物递送至淋巴结。这些研究提供了有价值的特征,包括大小、表面电荷、修饰、反应性、成分和细胞毒性,以实现淋巴结引流或细胞质进入的目标。
机器学习技术为探索这些纳米颗粒的理化特性和生物学特征提供了强大的工具,并促进了纳米载体的高效设计。通常,机器学习模型是通过高质量、海量的计算数据集和高通量实验数据来训练、选择和优化的,进而指导纳米载体的合理设计、筛选和优化。
通过利用现有的纳米载体数据库,机器学习可以为高效纳米疫苗的合理设计提供见解。
在《国家科学评论》发表的一篇新研究文章中,来自中国科学院和上海交通大学的科学家利用机器学习来指导mRNA纳米疫苗的合理化设计。这项研究基于纳米载体数据库的机器学习模型,确定了纳米疫苗有效递送mRNA和cGAMP的关键参数。
制备了基于苯硼酸接枝聚乙烯亚胺的mRNA/cGAMP纳米复合物,并进一步用阴离子脂质封装,得到纳米疫苗。
(1)纳米疫苗的负表面电荷减少了与基质中带负电荷的糖胺聚糖的相互作用,并改善了在淋巴结中的积累。
(2)纳米疫苗被抗原呈递细胞内化后淋巴结中的抗原呈递细胞(APC)内化后,促进mRNA和cGAMP从内体释放到细胞质,从而激活STING通路并诱导肿瘤抗原的呈递
(3)STING通路的激活促进IFN-I的释放,从而激活T细胞免疫反应杀死肿瘤细胞,抑制肿瘤的生长和转移。与单独的mRNA相比,基于这种纳米疫苗的治疗策略在黑色素瘤和结直肠癌模型中表现出更强的抗肿瘤作用。
版权说明:本站所有作品图文均由用户自行上传分享,仅供网友学习交流。若您的权利被侵害,请联系我们
相关文章:
- 2023-11-26研究表明南极臭氧层空洞在仲春时更深
- 2023-11-24机器人假肢脚踝改善自然运动和稳定性
- 2023-11-24球形机器人来救援
- 2023-11-24解释人工智能的方法可能并不那么容易解释
- 2023-11-24描述开放系统中量子信息加扰的通用框架
- 2023-11-24研究为抗生素耐药性和健身景观提供了新的见解
- 2023-11-24物理学家发现量子材料中奇异电荷传输的证据
- 2023-11-23一种高效去除水产养殖废水中磷酸盐的方法
- 2023-11-23研究人员在防止钒电池容量损失方面获得了有希望的结果
- 2023-11-23了解化学处理沙土的强度发展机制
- 站长推荐
- 栏目推荐
- 阅读排行
- 健康和教育密切相关新西兰需要将其更多地融入小学
- Steam现已全面支持DualShock和DualSense控制器无需购买新的Xbox控制器
- DistrictTaco希望扩大其在罗利地区的业务
- Humane的AiPin–您的新型可穿戴人工智能助手
- Microsoft365CopilotAI如何提高您的工作效率
- MicrosoftRadius云开源应用程序平台
- 生产目的FiskerPear具有透明A柱因为移动头部太困难
- 索尼Xperia5V马来西亚发布Snapdragon8Gen2SoC 8GBRAM 256GB储存空间起价RM4999
- Nissan的模块化PulsarSportbak集轿跑车 旅行车和皮卡于一体
- 新奥尔良烤肉店将在中央市场推出
